Бутиллітій
Бутиллітій — металоорганічна сполука, що використовується як ініціатор полімеризації, а також як реагент в органічному синтезі.
| n-Бутиллітій | |
|---|---|
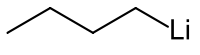 | |
| Назва за IUPAC | n-Бутиллітій, |
| Інші назви | Бутиллітій, BuLi, 1-літійбутан |
| Ідентифікатори | |
| Номер CAS | 109-72-8 |
| PubChem | 61028 |
| Номер EINECS | 203-698-7 |
| ChEBI | 51469 |
| SMILES |
CCCC[Li] |
| InChI |
1/C4H9.Li/c1-3-4-2;/h1,3-4H2,2H3;/rC4H9Li/c1-2-3-4-5/h2-4H2,1H3 |
| Номер Бельштейна | 1209227 |
| Номер Гмеліна | 1846 |
| Властивості | |
| Молекулярна формула | C4H9Li |
| Молярна маса | 64,06 г/моль |
| Зовнішній вигляд | безбарвна рідина, нестійка, переважно зберігається як розчин в аполярних розчинниках |
| Густина | 0.68 г/см3 (розчин в гексані, визанчається розчинником) |
| Тпл | -76 |
| Ткип | розкладається |
| Розчинність (вода) | бурхливо реагує з водою |
| Розчинність | Diethyl ether, cyclohexane |
| Кислотність (pKa) | 50 [джерело?] |
| Структура | |
| Геометрія | В розчині може бути у формі тетрамеру |
| Небезпеки | |
| Головні небезпеки | може самозайматись на повітрі, гідролізується до LiOH |
| NFPA 704 |
 4
3
3
|
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Отримання
- 2Li + C4H9X → C4H9Li + LiX (X = Cl, Br)
Хімічні властивості
Реакції бутиллітію є типовими для аліфатичних літійорганічних сполук.
Як основа
Бутиллітій — сильна основа (pKa > 35) і реагує з водою, спиртами і з багатьма більш кислими вуглеводнями[1]
- BuLi + H2O → BuH + LiOH
- BuLi + EtOH → BuH + EtOLi
- BuLi + PhCCH → BuH + PhCCLi
Як карбаніон
Бутиллітій вступає в типові реакції карбаніонів і є більш активним в реакціях приєднання, ніж реактиви Гріньяра:
- BuLi + СО2 → BuCOOLi
- BuLi + Me2СО → BuMe2COH
Для отриманння кетонів реакцію доводиться проводити з амідами кислот:
- BuLi + R2CONMe2 → LiNMe2 + R2C(O)Bu
Обмін галогенів на метал
- BuLi + RCl → BuCl + RLi
Примітки
- Ulrich Wietelmann and Richard J. Bauer — Lithium and Lithium Compounds, Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a15_393
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.