Гідрид калію
Гідри́д ка́лію — неорганічна іонна сполука складу KH, речовина білого кольору.
| Гідрид калію | |
|---|---|
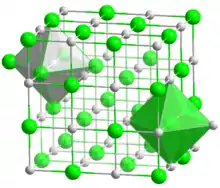 | |
| Систематична назва | Калій гідрид |
| Ідентифікатори | |
| Номер CAS | 7693-26-7 |
| Номер EINECS | 231-704-8 |
| ChEBI | 32589 |
| SMILES |
[H-].[K+][1] |
| InChI |
InChI=1S/K.H/q+1;-1 |
| Властивості | |
| Молекулярна формула | KH |
| Молярна маса | 40,106 г/моль |
| Густина | 1,43 г/см³[2] |
| Тпл | ~400 °C (розкл.)[2] |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Використовується як сильної основа для депротонування органічних кислоти та спиртів.
Хімічні властивості
Гідрид калію є дуже активною сполукою, відносно активнішою за гідрид натрію. Він бурхливо реагує з рідким аміаком та водою:
KH вступає в реакцію також і зі спиртовими розчинниками, утворюючи алкоголяти:
При високих температурах гідрид реагує з багатьма неметалами та їхніми оксидами:
Застосування
Гідрид калію використовують для депротонування органічних кислоти та спиртів. У складі подвійних гідридів, наприклад алюмогідриду калію, KH є ефективним відновником для органічного синтезу.
Див. також
Примітки
- Potassium hydride
- За тиску 101,3 кПа
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Рипан Р., Четяну И. Неорганическая химия: Химия металлов / В. И. Спицын. — М. : "Мир", 1971. — Т. 1. — 561 с. (рос.)
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.