Диметилформамід
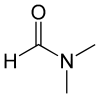
Димети́лформамі́д (іноді називають абревіатурою DMF або ДМФА, хоча акронім ДМФ іноді використовується для диметилфурану) — органічна сполука з формулою (CH3)2NC(O)H.
| Диметилформамід | |
|---|---|
 | |
 |
 |
| Назва за IUPAC | N,N-диметилформамід[1] |
| Інші назви | N,N-диметилметанамід[джерело?] |
| Ідентифікатори | |
| Номер CAS | 68-12-2 |
| PubChem | 6228 |
| Номер EINECS | 200-679-5 |
| DrugBank | DB01844 |
| KEGG | C03134 |
| Назва MeSH | Dimethylformamide |
| ChEBI | 17741 |
| RTECS | LQ2100000 |
| SMILES |
C[n](C):c:[o] |
| InChI |
InChI=1S/C3H7NO/c1-4(2)3-5/h3H,1-2H3 |
| Номер Бельштейна | 605365 |
| 3DMet | B00545 |
| Властивості | |
| Молекулярна формула | C3H7NO |
| Молярна маса | 73,09 г/моль |
| Зовнішній вигляд | Colourless liquid |
| Запах | fishy, ammoniacal |
| Густина | 0.948 g mL−1 |
| Розчинність (вода) | Miscible |
| Тиск насиченої пари | 516 Pa |
| Показник заломлення (nD) | 1.4305 (at 20 °C) |
| В'язкість | 0.92 mPa s (at 20 °C) |
| Структура | |
| Дипольний момент | 3.86 D |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
−240.6–−238.2 kJ mol−1 |
| Ст. ентальпія згоряння ΔcH |
−1.9428–−1.9404 MJ mol−1 |
| Теплоємність, c |
146.05 J K−1 mol−1 |
| Небезпеки | |
| ЛД50 |
|
| ГГС піктограми |   Шаблон:GHS health hazard Шаблон:GHS health hazard |
| ГГС формулювання небезпек | 226, 312, 319, 332, 360 |
| ГГС запобіжних заходів | 280, 305+351+338, 308+313 |
| Індекс ЄС | 616-001-00-X |
| Класифікація ЄС | |
| R-фрази | Шаблон:R61, Шаблон:R20/21, R36/37 |
| S-фрази | S45 |
| NFPA 704 |
 2
2
0
|
| Температура спалаху | 58 °C |
| Температура самозаймання | 445 °C |
| Вибухові границі | 2.2–15.2% |
| Пов'язані речовини | |
| Інші (alkanamides) |
|
| Пов'язані речовини |
|
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Отримання
ДМФА отримують реакцією диметиламіну з моноксидом вуглецю при нагріванні під високим тиском:
Іншим способом отримання є реакція диметиламіну з метилметаноатом (метиловим естером мурашиної кислоти) :
ДМФА очищають за допомогою вакуумного перегону, а чистоту контролюють за значенням питомої електричної провідності.[2]
Застосування
Завдяки доступності, інертності до конструкційних матеріалів та стійкості до гідролізу ДМФА знаходить широке застосування в промисловості, органічному синтезі, фармації.[3]
Примітки
- Dimethylformamide - Compound Summary. PubChem Compound. USA: National Center for Biotechnology Information. September 2004. Identification. Процитовано 28 червня 2012.
- Вайсбергер А., Проскауэр Э., Риддик Дж. Органические растворители. М.: Изд- во ИЛ, 1958
- Гончаров А. И., Корнилов М. Ю. Справочник по химии. Киев: Вища шк., 1978
- Hazardous substance fact sheet for Dimethylformamide
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.