Етенон
Етенон (кетен) — це найпростіший кетен з хімічною формулою . За кімтатної температури нестабільний.
| Етенон | |
|---|---|
| Назва за IUPAC | Етенон |
| Систематична назва | Етенон |
| Інші назви | Кетен |
| Ідентифікатори | |
| Номер CAS | 463-51-4 |
| Номер EINECS | 207-336-9 |
| Номер EC | 207-226-9 |
| ChEBI | 48003 |
| RTECS | OA7700000 |
| SMILES |
C=C=O |
| InChI |
1S/C2H2O/c1-2-3/h1H2 |
| Номер Бельштейна | 1098282 |
| Номер Гмеліна | 24996 |
| Властивості | |
| Молекулярна формула | C2H2O |
| Молярна маса | 42,04 г/моль |
| Молекулярна маса | 42 а. о. м. |
| Зовнішній вигляд | Безбарвна газ |
| Густина | 1,45 (відносна густина) |
| Тпл | -150 °C |
| Ткип | -41—-56 °C |
| Розчинність (ацетон) | легко розчинний |
| Розчинність (діетиловий етер) | легко розчинний |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-61,09 кДж/моль |
| Ст. ентальпія згоряння ΔcH |
1025,4 кДж/моль |
| Ст. ентропія S |
241,79 Дж/(моль*K) |
| Теплоємність, c |
51,76 Дж/(моль*K) |
| Небезпеки | |
| ГГС піктограми |     |
| ГГС формулювання небезпек | H220, H301, H315, H318, H319, H330, H335 |
| ГГС запобіжних заходів | P210, P260, P261, P264, P270, P271, P280, P284
,P301+310, P302+352, P304+340, P305+351+338, P310, P312, P320, P321 ,P330, P332+313, P337+313, P362, P377, P381, P403, P403+233 ,P405, P501 |
| Пов'язані речовини | |
| Пов'язані речовини | Дикетен |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Хімічні властивості
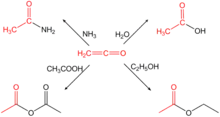
Етенон дуже хімічно активний.
Ацилювання
Реагує з багатьма нуклеофілами, ацилюючи їх. Він взаємодіє з водою, утворюючи оцтову кислоту:
Аналогічно взаємодіє зі спиртами, але в цій реакції утворюються естери:
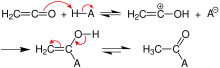
При взаємодії з оцтовою кислотою утворює оцтовий ангідрид:
Також ацилює аміак і аміни (окрім третинних), утворюючи аміди оцтової кислоти:
Циклоприєднання
При приєднанні різних сполук до подвійного зв'язку між атомами карбону кетену утворюються 4-членні циклічні сполуки. Прикладом такої реакції є димеризація кетену, яка відбувається за кімнатної температуи, утворюючи дикетен:
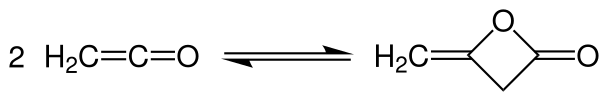
Ця реакція є прикладом приєднання карбонільних сполук, кнаслідок якої утоврюються лактони. Інша можлива реакція циклоприєднання — реакція з дієнами.
Отримання
Етенон отримують піролізом ацетону. Спочатку ацетон розпадається на CH3-CO та CH3, а потім атом гідрогену з першого радикалу переходить до другого, залишаючи кетен, та утворює метан:
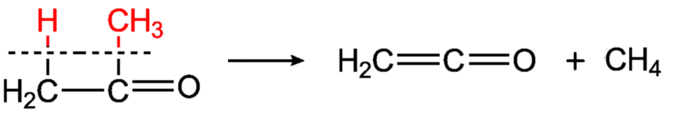
Також можна отримати дегідрогалогенуванням оцтового хлорангідриду. Для цього використовують сильні органічні основи, наприклад, третинні аміни:
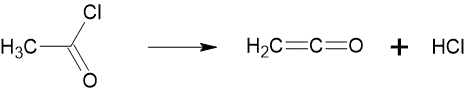
Джереда
Література
О. Я. Нейланд. Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1.
Miller, Raimund; Abaecherli, Claudio; Said, Adel; Jackson, Barry (2001). Ketenes. Ullmann's Encyclopedia of Industrial Chemistry (en). John Wiley & Sons, Ltd. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a15_063.