Оксид берилію
Окси́д бери́лію — неорганічна бінарна сполука Берилію та Оксигену складу BeO. Являє собою білі гексагональні кристали. Проявляє амфотерні властивості.
| Оксид берилію | |
|---|---|
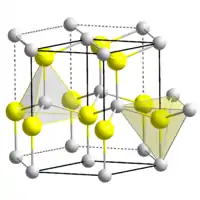 Кристалічна структура BeO | |
| Назва за IUPAC | Берилій оксид |
| Ідентифікатори | |
| Номер CAS | 1304-56-9 |
| Номер EINECS | 215-133-1 |
| ChEBI | 62842 |
| RTECS | DS4025000 |
| SMILES |
[Be]=O[1] |
| InChI |
InChI=1S/Be.O |
| Номер Бельштейна | 3902801 |
| Властивості | |
| Молекулярна формула | BeO |
| Молярна маса | 25,011 г/моль |
| Зовнішній вигляд | білі кристали |
| Густина | 3,01 г/см³[2] |
| Тпл | 2577 °C[2] |
| Розчинність (вода) | нерозчинний |
| Розчинність (кислоти) | розчинний |
| Розчинність (луги) | розчинний |
| Діелектрична проникність (ε) | 13,8 кВ/мм |
| Показник заломлення (nD) | 1,7184 |
| Структура | |
| Кристалічна структура | гексагональна |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-609,4 кДж/моль |
| Ст. ентропія S |
13,77 Дж/(моль·К) |
| Теплоємність, c |
25,6 Дж/(моль·К) |
| Пов'язані речовини | |
| Інші катіони | оксид алюмінію |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Завдяки своїй тугоплавкості застосовується для виготовлення тиглів та облицювання печей. Поширений у складі мінералів берилу, хризоберилу, фенакіту та гельвіну. Дана сполука є канцерогеном.
Поширення у природі
Оксид берилію поширений у природі переважно у вигляді силікатів. Найважливішими мінералами для добування BeO є берил, хризоберил, фенакіт та гельвін. Дещо менший вміст BeO спостерігається також у бромеліті, евклазі, даналіті.
Хімічні властивості
Оксид берилію не реагує з водою. Проявляє амфотерні властивості — взаємодіє як із кислотами, так і з лугами (та відповідними оксидами):
Оксид легко піддається флуоруванню:
За допомогою сильних відновників, наприклад, магнію чи графіту, берилій можна відновити з оксиду:
Отримання
Окрім добування з мінералів, оксид берилію також можна синтезувати в лабораторних умовах. Оксид утворюється в результаті згоряння металічного берилію на повітрі, а також при термічній дисоціації кисневмісних сполук берилію:
Безпека
Оксид берилію, як і інші його сполуки, належать до канцерогенів. Тривалий контакт зі сполукою здатен спричиняти появу берилієвої хвороби або бериліозу.
Застосування
Берилій оксид застосовують як каталізатор, а також як вогнетривкий матеріал для виготовлення тиглів та внутрішнього облицювання електричних печей.
Див. також
Примітки
- BERYLLIUM OXIDE
- За тиску 101,3 кПа
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Рипан Р., Четяну И. Неорганическая химия: Химия металлов / В. И. Спицын. — М. : "Мир", 1971. — Т. 1. — 561 с. (рос.)
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)
