Сіль Мора
Сіль Мора — це тривіальна назва амоній залізо (ІІ) сульфату гексагідрату, що має формулу (NH4)2Fe(SO4)2·6H2O і є сіллю у формі кристалогідрату. Поширений лабораторний реактив, який, як і більшість солей заліза (II), добре розчиняється у воді, з утворенням розчину забарвленого у світло-зелений колір аква-комплексу [Fe(H2O)6]2+, що має октаедричну структуру.[1]
| Сіль Мора | |
|---|---|
 | |
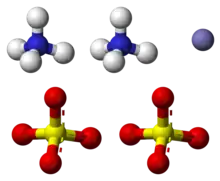 | |
 | |
| Назва за IUPAC | Залізо(II) амоній сульфат |
| Інші назви | Сіль Мора |
| Ідентифікатори | |
| Номер CAS | 10045-89-3 |
| PubChem | 24863 |
| Номер EINECS | 233-151-8 |
| ChEBI | 76243 |
| SMILES |
[Fe+2].[O-]S(=O)(=O)[O-].[O-]S([O-])(=O)=O.[NH4+].[NH4+] |
| InChI |
1/Fe.2H3N.2H2O4S/c;;;2·1-5(2,3)4/h;2·1H3;2*(H2,1,2,3,4)/q+2;;;;/p-2 |
| Номер Бельштейна | 13163104 |
| Властивості | |
| Молекулярна формула | (NH4)2Fe(SO4)2·6H2O |
| Молярна маса | 284,05 г/моль (anhydrous) 392,14 г/моль (hexahydrous) |
| Зовнішній вигляд | Зеленуваті кристали |
| Густина | 1,86 |
| Тпл | 100—110 °C |
| Небезпеки | |
| MSDS | Fisher MSDS |
| R-фрази | R36/37/38 |
| S-фрази | S24/25 |
| Головні небезпеки | |
| NFPA 704 |
 0
2
0
|
| Пов'язані речовини | |
| Пов'язані речовини | Залізо-амонійні галуни |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Застосування
В аналітичній хімії, ця сіль використовується замість сульфату заліза (II) для титриметрії, оскільки на повітрі вона не окиснюється до заліза(III). Окиснення розчинів заліза(II) є дуже pH-залежним, швидкість окиснення є вищою за високих pH. Іони амонію надають розчину солі Мора слабко-кислу реакцію, що уповільнює окиснення.
Сіль Мора названо на честь німецького хіміка Карла Фрідріха Мора, що розробив багато методів титриметрії у XIX столітті. Відомі схожі солі, наприклад солі Туттона.
Отримання солі Мора
Сіль Мора виготовляють розчиненням еквімолярних кількостей гідратів залізо(II) сульфату та амоній сульфату у воді, що містить невелику кількість сірчаної кислоти, з наступним упарюванням розчину до кристалізації. Залізо-амоній сульфат утворює зелені кристали гідрату.
Кристалічна форма
Кристали солі Мора мають моноклінну сингонію.