трет-Бутанол
трет-Бутанол (трет-бутиловий спирт) — найпростіший третинний спирт. Його хімічна формула (CH3)3COH (інколи записується t-BuOH). трет-Бутанол є одним з чотирьох ізомерних бутанолів. Це — безбарвна рідина з камфороподібним запахом, що замерзає при температурі, близькій до кімнатної. Вона змішується з водою, етанолом та більшістю органічних розчинниках в будь-яких співвідношеннях.
| трет-бутанол | |
|---|---|
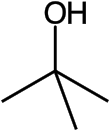 Структурна формула трет-бутанолу |
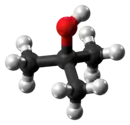 Кулько-стержнева модель молекули трет-бутанолу |
 Частково кристалізовний трет-бутанол | |
| Інші назви | Шаблон:Bulletedlist |
| Ідентифікатори | |
| Номер CAS | 75-65-0 |
| PubChem | 6386 |
| Номер EINECS | 200-889-7 |
| DrugBank | DB03900 |
| Назва MeSH | tert-Butyl+Alcohol |
| ChEBI | 45895 |
| RTECS | EO1925000 |
| SMILES |
CC(C)(C)O |
| InChI |
InChI=1S/C4H10O/c1-4(2,3)5/h5H,1-3H3 |
| Номер Бельштейна | 906698 |
| Номер Гмеліна | 1833 |
| Властивості | |
| Молекулярна формула | C4H10O |
| Молярна маса | 74,12 г/моль |
| Зовнішній вигляд | Безбарвна рідина, що замерзає при близькій до кімнатної теператури |
| Запах | Схожий на запах камфори |
| Густина | 0,775 г/мл |
| Розчинність (вода) | змішується[1] |
| Тиск насиченої пари | 4,1 кПа (при 20 °C) |
| Кислотність (pKa) | 16,54 [2] |
| Показник заломлення (nD) | 1,387 |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
−360,04...−358,6 кДж/моль |
| Ст. ентальпія згоряння ΔcH |
−2,64479–−2,64321 МДж/моль |
| Ст. ентропія S |
189,5 Дж/(моль·K) |
| Теплоємність, c |
215,37 Дж/(моль·K) |
| Небезпеки | |
| ГДК (США) | TWA 100 ppm (300 мг/м3)[3] |
| ЛД50 | 3559 мг/кг (кролики, перорально) 3500 мг/кг (щури, перорально)[4] |
| ГГС піктограми |   |
| ГГС формулювання небезпек | 225, 319, 332, 335 |
| ГГС запобіжних заходів | 210, 261, 305+351+338 |
| Класифікація ЄС | |
| R-фрази | R11, R20
, R36/37 |
| S-фрази | S2, S9, S16, Шаблон:S46 |
| NFPA 704 |
 3
1
0
|
| Вибухові границі | 2,4–8,0 % |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Отримання
В промисловості трет-бутанол отримують з ізобутану як побічний продукт при синтезі оксиду пропілену. Також його можна отримати каталітичним приєднанням води до ізобутену:
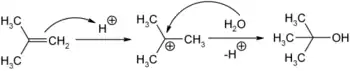 Синтез 2-метил-2-пропанолу з ізобутену
Синтез 2-метил-2-пропанолу з ізобутену
Проста перегонка не дозволяє отримати чистий трет-бутанол оскільки він утворює азеотроп з водою, тим не менше, в в промисловості початкову очистку трет-бутанолу від води проводять додаванням бензену і перегонкою трьохкомпонентної суміші (відгонка азеотрпу трет-бутанол-вода-бензен). Менші кількості води видаляють сушкою над CaO, K2CO3, CaSO4 чи MgSO4 з наступною відгонкою. Безводний трет-бутанол отримують подальшою перегонкою з додаванням металічного магнію активованого йодом чи лужними металами. Альтернативно можна використовувати 4 Å молекулярні сита, CaH2 чи навіть фракційну кристалізацію в інертній атмосфері.[5]
Використання
трет-Бутанол використовується як розчинник, як денатуруюча добавка до етанолу, як добавка до пального для підняття октанового числа, він також входить до складу деяких сумішей для зняття фарб. трет-Бутанол є проміжною сполукою при синтезі метил-трет-бутилового естеру (MTBE) і трет-бутилгідропероксиду (TBHP).
Реакції
трет-Бутанол може бути депротонований сильними основами утворюючи трет-бутоксил-аніон. Наприклад, кип'ятіння трет-бутанолу з металічним калієм дозволяє отримати типовий реагент органічного синтезу tBuOK[6]
- K + tBuOH → tBuO−K+ + 0,5H2
Примітки
- http://www.inchem.org/documents/icsc/icsc/eics0114.htm
- Reeve, W.; Erikson, C.M.; Aluotto, P.F. Can. J. Chem, 1979, 57, 2747.
- NIOSH Pocket Guide to Chemical Hazards #0078. Національний інститут охорони праці (NIOSH).
- «tert-Butyl alcohol». Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- D.D. Perrin, W.L.F. Armarego (1988). Purification of Laboratory Chemicals (вид. 3rd). Pergamon Press Ltd.
- Johnson, W. S.; Schneider, W. P. (1950). β-Carbethoxy-γ,γ-diphenylvinylacetic acid. Org. Synth. 30: 18.; Coll. Vol. 4: 132.