Циклопропан
Ци́клопропа́н (лат. Cyclopropanum) — найпростіша органічна речовина класу циклоалканів. Хімічна формула — C3H6.
| Циклопропан[1] | |
|---|---|
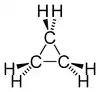 Cyclopropane - displayed formula |
Cyclopropane - skeletal formula |
 {{{ImageAltL2}}} |
 |
| Назва за IUPAC | Cyclopropane |
| Ідентифікатори | |
| Номер CAS | 75-19-4 |
| PubChem | 6351 |
| Номер EINECS | 200-847-8 |
| DrugBank | 13984 |
| KEGG | D03627 |
| ChEBI | 30365 |
| SMILES |
C1CC1 |
| InChI |
1/C3H6/c1-2-3-1/h1-3H2 |
| Номер Бельштейна | 605256 |
| Номер Гмеліна | 635 |
| Властивості | |
| Молекулярна формула | C3H6 |
| Молярна маса | 42,08 г/моль |
| Густина | 1,879 г/л (1 atm, 0 °C) |
| Тпл | -128 |
| Ткип | -33 |
| Небезпеки | |
| MSDS | External MSDS |
| ГГС піктограми |  |
| ГГС формулювання небезпек | 220 |
| ГГС запобіжних заходів | 210, 377, 381, 403 |
| NFPA 704 |
 4
1
0
|
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Фізичні властивості
Безбарвний горючий газ з характерним запахом, що нагадує запах петролейного ефіру, їдкого на смак. Відносна густина 1,879. При температурі 4—20 °C і тиску 5 атм переходить у рідкий стан; температура плавлення −127 °C, температура кипіння циклопропану при атмосферному тиску −33 °C. Малорозчинний у воді (один об'єм газу при + 20 ° C розчинний в 2,85 об'єму води). Легкорозчинний у спирті, петролейному ефірі, хлороформі та жирних оліях. Легко загоряється. Суміші з повітрям, киснем або оксидом азоту(I) вибухонебезпечні.
Циклопропан (як і циклобутан) можна отримати за допомогою внутрішньомолекулярної реакції Вюрца з α, ω-дигалогеналканів при нагріванні з металами (Na, Mg, Zn):
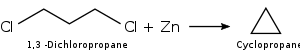
Хімічні властивості
Вступає у реакцію з воднем з утворенням пропану:
Реагує з кислотами. При цьому протон приєднується до третього атома карбону, а кислотний залишок до першого. Наприклад:
З галогеноводневими кислотами утворює галогенпропан:
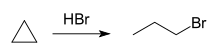
З сульфатною кислотою утворює пропілсульфатну кислоту:
Реагує з галогенами, утворюючи 1,3-дигалогенпропан:
При низькій температурі хлор може витісняти один з атомів гідрогену:
При високій температурі у присутності заліза або платини перетворюється на пропілен:
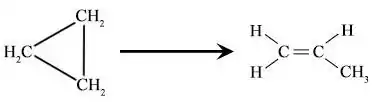
Застосування
У минулому використовувався як засіб для наркозу у 15—30% суміші з киснем та іншими газами. Внаслідок високої небезпеки вибуху та негативного впливу на серце замінюють іншими препаратами.
Примітки
- Merck Index, 11th Edition, 2755.
Література
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — 560 с. — ISBN 978-966-382-113-9. (С.132,198,199)
- Д.Г.Кузнецов Органическая химия 13358K, 556 с. издание 2016 г. (С.?)