Оксид урану(V,VI)
Окси́д ура́ну(V,VI) — неорганічна сполука, змішаний оксид складу U3O8 (або U2O5·UO3). Має вигляд зеленувато-чорних кристалів.
| Оксид урану(V,VI) | |
|---|---|
 | |
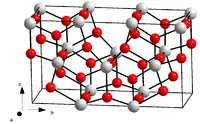 | |
| Систематична назва | Уран(V,VI) оксид |
| Інші назви | Триурану октаоксид, оксид урану(VI)-диурану(V) |
| Ідентифікатори | |
| Номер CAS | 1344-59-8 |
| Номер EINECS | 215-702-4 |
| SMILES | |
| InChI |
InChI=1S/8O.3U |
| Властивості | |
| Молекулярна формула | U3O8 |
| Молярна маса | 842,082 г/моль |
| Зовнішній вигляд | зелено-чорні кристали |
| Густина | 8,38 г/см³ |
| Тпл | 1150 °C |
| Ткип | 1300 °C (розкл.) |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-3574,8 кДж/моль |
| Ст. ентропія S |
282,55 Дж/(моль·K) |
| Теплоємність, c |
42,74 Дж/(моль·K) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Оксид має чотири модифікації: α, α', α'', β. Густина у різних формах змінюється у діапазоні 8,16—8,41 г/см³.
Отримання
Добування сполуки проводиться шляхом термічного розкладання ряду сполук, зокрема, (NH4)2U4O13, UO4·xH2O, UO2(NO3)2·6H2O при 600 °C, окисненням UO2 у струмені повітря при 600 °C.
Хімічні властивості
За високих температур (на повітрі при 900 °C, а у вакуумі вже при 600 °C) оксид U3O8 починає розкладатися із утворенням оксиду UO2, з яким утворює тверді розчини:
U3O8 повільно розчиняється у кислотах-окисниках, повністю окиснюючись до стану U(VI) та гідролізуючись до сполук уранілу UO22+. При пропусканні хлороводню крізь оксид при температурі 700 °C утворюється ураніл хлорид.
При дії пероксиду водню сполука активно окиснюється до пероксиду урану:
За температури понад 500 °C U3O8 відновлюється воднем або амоніаком до діоксиду.
Застосування
Оксид урану(V,VI) використовується як добавка для розкладання органічних сполук (бензену, бутану), як компонент каталізаторів у риформінгу. Він є вихідною сировиною для отримання гранульованого діоксиду урану, що використовується як ядерне паливо, також U3O8 використовується як паливо й безпосередньо.
Див. також
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Myers Richard L. The 100 Most Important Chemical Compounds. — Westport, CT : Greenwood Press, 2007. — 326 p. — ISBN 978-0-313-33758-1. (англ.)
- Clark D. L., Neu M. P., Runde W., Keogh D. W. Uranium and Uranium Compounds // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. 24. — P. 324. — ISBN 978-0-471-48517-9. — DOI: (англ.)
- Peehs M., Walter T., Walter S., Zemek M. Uranium Compounds // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — P. 49—50. — DOI: (англ.)
- Реми Г. Курс неорганической химии / Под ред. А. В. Новоселовой. — М. : ИИЛ, 1966. — Т. 2. — 833 с. (рос.)