Трифенілфосфін
Трифенілфосфі́н (назва за ІЮПАК — трифенілфосфа́н) — фосфорорганічна сполуках з хімічною формулою P(C6H5)3, часто скорочується до PPh3 або Ph3P. Трифенілфосфін широко використовується в синтезі органічних і металоорганічних сполук. За нормальних умов, PPh3 — це безбарвні, відносно стабільні на повітрі кристали, які розчиняються в неполярних органічних розчинниках, таких як бензен і діетиловий ефір.
| Трифенілфосфін | |
|---|---|
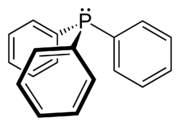 Структурна будова | |
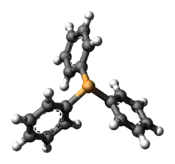 Кульково-сірникова модель молекули трифенілфосфіну | |
 | |
| Назва за IUPAC | Трифенілфосфан |
| Ідентифікатори | |
| Номер CAS | 603-35-0 |
| PubChem | 11776 |
| Номер EINECS | 210-036-0 |
| RTECS | SZ3500000 |
| SMILES |
c3c(P(c1ccccc1)c2ccccc2)cccc3 |
| InChI |
1/C18H15P/c1-4-10-16(11-5-1)19(17-12-6-2-7-13-17)18-14-8-3-9-15-18/h1-15H |
| Властивості | |
| Молекулярна формула | C18H15P |
| Молярна маса | 262,29 г/моль |
| Зовнішній вигляд | Білі кристали |
| Густина | 1,1 г/см3 |
| Тпл | 80 |
| Ткип | 377 |
| Розчинність (вода) | нерозчинний |
| Показник заломлення (nD) | 1,59 |
| Структура | |
| Геометрія | пірамідальна |
| Дипольний момент | 1,4 - 1,44 Д [1] |
| Небезпеки | |
| MSDS | JT Baker |
| Класифікація ЄС | Не значиться |
| R-фрази | R20
R22R40R43R50Шаблон:R53 |
| S-фрази | S36S37S45Шаблон:S57S60 |
| Температура спалаху | 180 °C |
| Пов'язані речовини | |
| Інші (третинні фосфіни) | триметилфосфін фосфін |
| Пов'язані речовини | Трифеніламін Трифеніларсин Оксид трифенілфосфіну Сульфід трифенілфосфіну Хлорид трифенілфосфіну |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Отримання
В лабораторних умовах трифеніл фосфін може бути отриманий шляхом взаємодії трихлориду фосфору з фенілмагнійбромідом або феніллітієм. В промисловості трифенілфосфін отримують шляхом взаємодії трихлориду фосфору, хлорбензолу та натрію.
Застосування
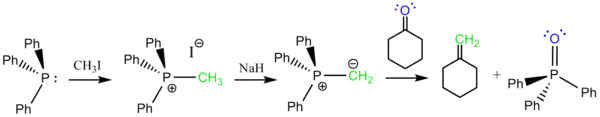
У реакції Віттіга
Трифенілфосфін є одним з вихідних реагентів реакції Віттіга, реакції між карбонільною сполукою та фосфонієвим ілідом з утворенням алкену. Фосфонієві іліди утворюються при депротонуванні фосфонієвих солей сильною основою. Фосфонієві солі, в свою чергу утворюють з трифенілфосфіну та алкілгалогеніду.
Див. також
- Реакція Віттіга
- Реакція Аппеля
Примітки
- Warchol, M.; Dicarlo, E. N.; Maryanoff, C. A.; Mislow, K. Evidence for the contribution of the lone pair to the molecular dipole moment of triarylphosphines // Tetrahedron Letters. — 1975. — Т. 16, вип. 11 (25 листопада). — С. 917–999. — DOI:. Процитовано 07.06.2012.
Джерела
- Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — ISBN 966-7022-19-6.
- Clayden J., Greeves N., Warren S. Organic chemistry. — 2nd ed. — Oxford University Press, 2012. — ISBN 978-0-19-927029-3.