1,4-Бензохінон
1,4-Бензохінон (п-бензохінон) — органічна сполука з класу хінонів, має хімічну формулу O=C6H4=O[1]. Є жовтою кристалічною речовиною, яка сублімується при нагріванні[2].
| Структурна формула | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
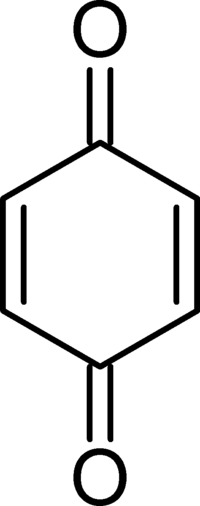 | ||||||||||||||||
| Загальна інформація | ||||||||||||||||
| Преференційна назва ІЮПАК | ||||||||||||||||
| Систематична назва ІЮПАК | циклогекса-2,5-дієн-1,4-діон | |||||||||||||||
| Інші назви |
1,4-Бензохінон, хінон, пара-бензохінон | |||||||||||||||
| Хімічна формула | C6H4O2 | |||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | |||||||||||||||
| Зовнішні ідентифікатори / Бази даних | ||||||||||||||||
| ||||||||||||||||
| Властивості | ||||||||||||||||
| Молярна маса | 108,021129 г/моль | |||||||||||||||
| Агрегатний стан |
Твердий | |||||||||||||||
| Зовнішній вигляд |
Жовті кристали | |||||||||||||||
| Температура плавлення |
115,7 °C | |||||||||||||||
| Температура кипіння |
180 °C | |||||||||||||||
| Температура самозаймання |
560 °C | |||||||||||||||
| Безпека | ||||||||||||||||
| Маркування згідно системі УГС
Небезпека | ||||||||||||||||
| H-фрази | H: H301, H315, H319, H331, H335, H400 | |||||||||||||||
| P-фрази | P: P261, P264, P270, P271, P273, P280, P301+P310, P302+P352, P304+P340, P305+P351+P338, P311, P312, P321, P330, P332+P313, P337+P313, P391, P403+P233, P405, P501 | |||||||||||||||
| LD50 |
25 мг/кг (миші, орально) | |||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | ||||||||||||||||
Фізичні властивості
Блідно-жовті кристали. Запах їдкий, схожий на запах хлору. Розчинний у спирті та етері[3], погано розчинний у воді. При нагріванні сублімується[2].

Отримання
Найперший метод отримання — окиснення природної хінної кислоти[1]:
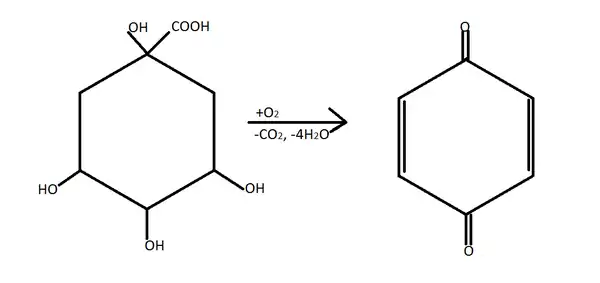
Пара-бензохінон також утворюється при окисненні гідрохінону[1]:
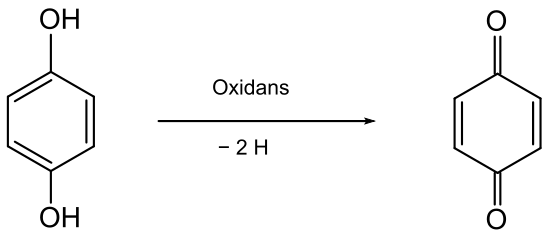
Ще один метод отримання — окиснення аніліну або п-діамінобензену[1]:
Хімічні властивості
Відновлення
Бензохінон є окисником. Може відновлюватися до гідрохінону, а при взаємодії з останнім утворює хінгідрон — комплекс бензохінону та гідрохінону з переносом заряду[1]:
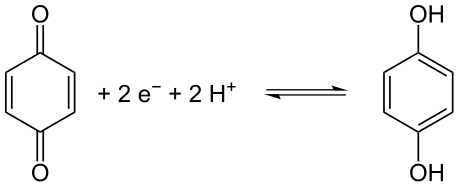
Спочатку приєднуються електрони з утворенням аніон-радикалу, який пізніше відновлюється до діаніону. В кінці діаніон приєднує протони[1]:
Ця реакція є оборотною, оскільки гідрохінон є сильним відновником.
Нуклеофільне приєднання
При нуклеофільному приєднанні також утворюється ароматична структура. Продукти цих реакцій — похідні гідрохінону[1]:
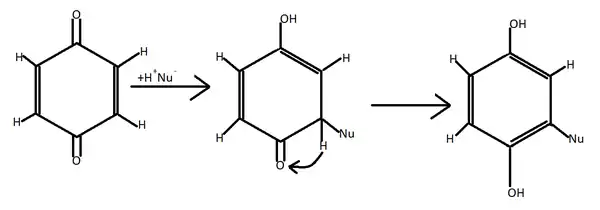
Реакції кетонів
Може давати похідні кетонів при взаємодії з відповідними сполуками. Наприклад, при взаємодії з гідроксиламіном утворюється оксим. Внаслідок нітрозо-оксимної таутомерії частина цього оксиму перетворюється на п-нітрозофенол[1]:
При більшій кількості гідроксиламіну утворюється діоксим, який, завдяки таутомерії, частково перетворюється на п-нітрозофенілгідроксиламін[1]:
Дієновий синтез
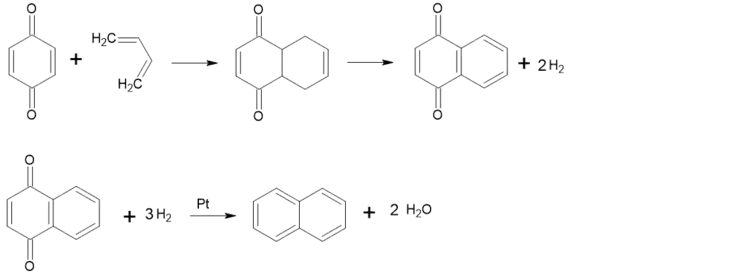
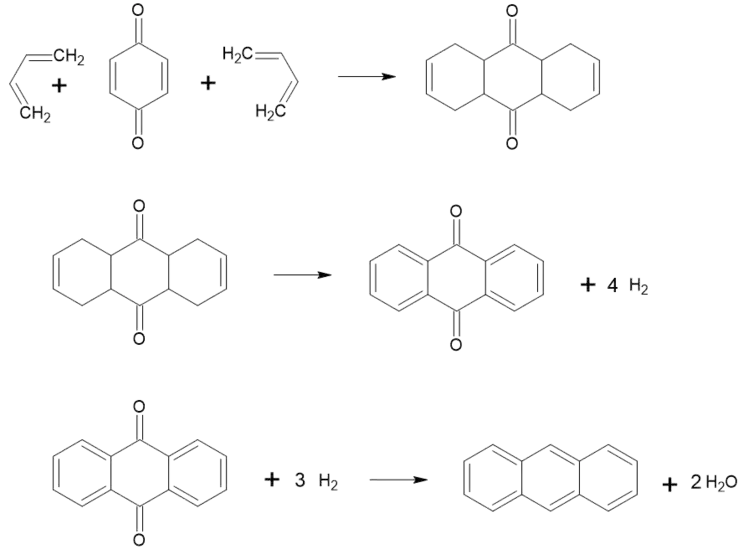
Як і інші хінони, є дієнофілом. При взаємодії з бутадієном утворюється тетрагідронафтохінон, який при дегідрогенуванні дає 1,4-нафтахінон. При відновленні останнього утворюється нафтален, що і використовується для його синтезу. При більшій кількості бутадієну він приєднується і до іншого подвійного зв'язку, утворюючи октагідроантрахінон, який теж дегідрують, відновлюють і в кінці отримують антрацен:
Примітки
- Ластухін, Юрій Олександрович; Воронов, Станіслав Андрійович (2009). Органічна хімія. Львів: Центр Європи. с. 723–725. ISBN 966-7022-19-6.
- CDC - NIOSH Pocket Guide to Chemical Hazards - Quinone. www.cdc.gov. Процитовано 26 вересня 2020.
- PubChem. Hazardous Substances Data Bank (HSDB) : 1111. pubchem.ncbi.nlm.nih.gov (англ.). Процитовано 27 вересня 2020.