4-амінонафтален-1-сульфокислота
4-амінонафтален-1-сульфокислота (нафтіонова кислота) — органічна сполука з класу сульфокислот і ароматичних амінів. Є білою твердою речовиною, яка погано розчинна у воді.[1]
| Структурна формула | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
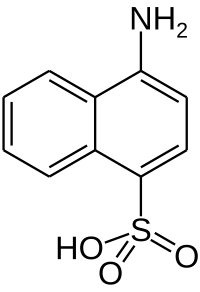 | |||||||||||||||||||
| Загальна інформація | |||||||||||||||||||
| Преференційна назва ІЮПАК | 4-амінонафтален-1-сульфокислота | ||||||||||||||||||
| Систематична назва ІЮПАК | 4-амінонафтален-1-сульфокислота | ||||||||||||||||||
| Інші назви |
нафтіонова кислота | ||||||||||||||||||
| Хімічна формула | C10H9NO3S | ||||||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | ||||||||||||||||||
| Зовнішні ідентифікатори / Бази даних | |||||||||||||||||||
| |||||||||||||||||||
| Властивості | |||||||||||||||||||
| Молярна маса | 223,25 г/моль [1] | ||||||||||||||||||
| Агрегатний стан |
Твердий [1] | ||||||||||||||||||
| Густина |
1,67 г/см3 (20 °C) [1] | ||||||||||||||||||
| Розчинність |
0,31 г/л (вода, 20 °С) [1] | ||||||||||||||||||
| Безпека | |||||||||||||||||||
| Маркування згідно системі УГС
Небезпека | |||||||||||||||||||
| H-фрази | H: H314 | ||||||||||||||||||
| P-фрази | P: P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P405, P501 | ||||||||||||||||||
| LD50 |
>7500 мг/кг (щур, орально) | ||||||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | |||||||||||||||||||
Отримання
Уперше була отримана сульфуванням та відновленням 1-нітронафталену сульфітом амонію, але при цьому утворювалися також ди- і три-сульфонові кислоти.[2]
Зараз застосовують такий спосіб: 1-нафтиламін розчиняють в 1,2-дихлоробензені, додається концентрована сульфатна кислота, отримана сіль нагрівається до 180°C з утворенням нафтіонової кислоти та води, вода відганяється, залишок додають до розчину натрій карбонату, водну фазу відділяють, натрій нафтіонат відділяють додаванням натрій хлориду, продукт відфільтровують.[2]
Хімічні властивості
У присутності гідрогенсульфіту натрію вступає в реакцію, протилежну реакції Бухерера з утворенням 4-гідроксинафталенсульфокислоти. Може вступати в реакції електрофільного заміщення, наприклад, реакція з діазосполуками утворює азобарвники.
Застосування
Застосовується для синтезу барвників, таких як конго червоний.[3]
Примітки
- GESTIS-Stoffdatenbank. gestis.dguv.de. Процитовано 21 квітня 2021.
- Booth, Gerald (15 червня 2000). У Wiley-VCH Verlag GmbH & Co. KGaA. Naphthalene Derivatives. Ullmann's Encyclopedia of Industrial Chemistry (англ.). Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. с. a17_009. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a17_009.
- Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — ISBN 966-7022-19-6.