Трифенілфосфаноксид
Трифенілфосфанокси́д (англ. triphenylphosphine oxide) — органічна сполука фосфору. Ця сполука зазвичай зустрічається в якості продукту реакцій трифенілфосфіну, але може також використовуватись як окисник у деяких реакціях.
| Структурна формула | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
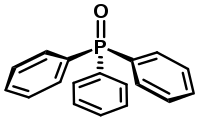  | |||||||||||||||||||||||||
| Загальна інформація | |||||||||||||||||||||||||
| Преференційна назва ІЮПАК | Трифенілфосфаноксид | ||||||||||||||||||||||||
| Систематична назва ІЮПАК | Трифенілфосфан-P-оксид | ||||||||||||||||||||||||
| Інші назви |
| ||||||||||||||||||||||||
| Хімічна формула | C18H15OP | ||||||||||||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | ||||||||||||||||||||||||
| Зовнішні ідентифікатори / Бази даних | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Властивості | |||||||||||||||||||||||||
| Молярна маса | 278.29 г·моль−1 | ||||||||||||||||||||||||
| Агрегатний стан |
Тверда речовина | ||||||||||||||||||||||||
| Зовнішній вигляд |
Кристали без кольору й запаху | ||||||||||||||||||||||||
| Густина |
1.2 г·см-3 (20 °C)[1] | ||||||||||||||||||||||||
| Температура плавлення |
155–158 °C[1] | ||||||||||||||||||||||||
| Температура кипіння |
>360 °C[1] | ||||||||||||||||||||||||
| Температура самозаймання |
590 °C[1] | ||||||||||||||||||||||||
| Розчинність |
Погано розчиняється в воді[1] | ||||||||||||||||||||||||
| Безпека | |||||||||||||||||||||||||
| Маркування згідно системі УГС
Увага | |||||||||||||||||||||||||
| H-фрази | H: H302, H412 | ||||||||||||||||||||||||
| P-фрази | P: P273 | ||||||||||||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | |||||||||||||||||||||||||
Одержання
Зазвичай трифенілфосфаноксид можна отримати в якості (стехіометричного) копродукту в деяких реакціях; найвідомішою є реакція Віттіга — взаємодія оксо-сполуки з фосфонієвим ілідом. Також він зустрічається серед продуктів інших реакцій, що використовують трифенілфосфан або його похідні: наприклад, у реакції Аппеля, реакції Штаудінгера, реакції Міцунобу.
Альтернативно трифенілфосфаноксид можна отримати шляхом окиснення трифенілфосфану; для цього підійдуть будь-які достатньо сильні окисники, наприклад, йод. Кисень повітря також окислює трифенілфосфан, тому останній завжди містить значну частку оксиду після тривалого зберігання.
Властивості
nickel(II)-from-xtal-3D-balls.png.webp)
Трифенілфосфаноксид погано розчиняється в воді, циклогексані, тетрахлорометані й ацетонітрилі . Однак він добре розчинний у дихлорметані, хлороформі та коротколанцюгових спиртах, таких як метанол, етанол й н-пропанол.[2]
Зв'язок P=O дуже поляризований й через велику різницю в енергіях орбіталей атомів має скоріше цвіттер-іонний характер, аніж характер подвійного зв'язку; подібний характер спостерігається також, наприклад, у диметилсульфоксиді, тому ці сполуки можна формально віднести до ілідів.[3]
Трифенілфосфаноксид є хорошим лігандом у комплексах жорстких металів, наприклад, NiCl2(OPPh3)2.[4]
Примітки
- Внесок про трифенілфосфаноксид у базі даних GESTIS
- E. Maccarone, G. Perrini, Gazz. Chim. Ital. 1982, 112, 447–454.
- IUPAC - ylides (Y06728). goldbook.iupac.org. Процитовано 23 січня 2020.
- D. M. L. Goodgame, M. Goodgame: Near-Infrared Spectra of Some Pseudotetrahedral Complexes of Cobalt (II) and Nickel(II), Inorg. Chem. 1965, 4, 139–143.
