2-нітрофенол
2-нітрофенол (орто-нітрофенол) ― органічна сполука з класу нітрофенолів. Є ізомером 3-нітрофенолу та 4-нітрофенолу.
| Структурна формула | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
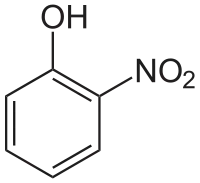 | ||||||||||||||||
| Загальна інформація | ||||||||||||||||
| Преференційна назва ІЮПАК | 2-нітрофенол | |||||||||||||||
| Систематична назва ІЮПАК | 2-нітрофенол | |||||||||||||||
| Інші назви |
орто-нітрофенол, 1-гідрокси-2-нітробензен | |||||||||||||||
| Хімічна формула | C6H5NO3 | |||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | |||||||||||||||
| Зовнішні ідентифікатори / Бази даних | ||||||||||||||||
| ||||||||||||||||
| Властивості | ||||||||||||||||
| Молярна маса | 139,11 г/моль [1] | |||||||||||||||
| Агрегатний стан |
Твердий [1] | |||||||||||||||
| Густина |
1,495 г/см3 (20 °C) [1] | |||||||||||||||
| Температура плавлення |
44 °C [1] | |||||||||||||||
| Температура кипіння |
214 °C [1] | |||||||||||||||
| Температура самозаймання |
550 °C [1] | |||||||||||||||
| Розчинність |
2,1 г/л (H20, 20 °C) [1] | |||||||||||||||
| Безпека | ||||||||||||||||
| Маркування згідно системі УГС
Увага | ||||||||||||||||
| H-фрази | H: H302, H312, H332, H400, H410 | |||||||||||||||
| P-фрази | P: P273, P280, P302+P352, P304+P340, P305+P351+P338, P312 | |||||||||||||||
| EUH-фрази | EUH: Заходи безпеки відсутні | |||||||||||||||
| LD50 |
334 мг/кг (щур, орально) [1] | |||||||||||||||
| Вибухонебезпечність | ||||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | ||||||||||||||||
Фізичні властивості
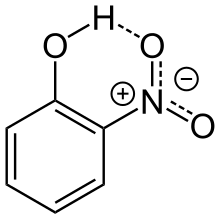
За стандартних умов є жовтою кристалічною речовиною, кристали мають вигляд голок. Погано розчиняється в воді. На відміну від 4-нітрофенолу, 2-нітрофенол летючий. Це пов'язано з тим, що у молекулах 2-нітрофенолу утворюються внутрішньомолекулярні водннві зв'язки замість міжмолекулярних, як у 4-нітрофенолу.[2]
Отримання
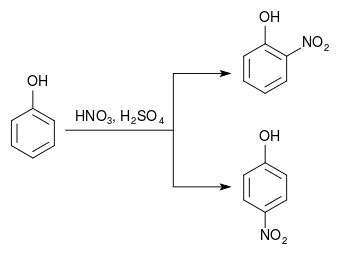
Нітруванням фенолу
При нітруванні фенолу утворюється суміш 2-нітрофенолу та 4-нітрофенолу. Оскільки 2-нітрофенол більш летючий, ніж 4-нітрофенол, продукти можна розділити дистиляцією.[2]
Гідролізом 4-хлоронітробензену
Гідроліз 2-хлоронітробензену економічно вигідніший за нітрування фенолу, тому саме ця реакція є основним джерелом одержання 2-нітрофенолу. Проврдять реакцію наступним чином: 2-хлоронітробензен розчиняють у 8,5% розчині гідроксиду натрію, поступово нагрівають до 170 °С та тримають в автоклаві протягом 8 годин.[2]
Застосування
Застосовують для отримання 2-амінофенолу.[2]
Токсичність
2-нітрофенолу може викликати незначне подразнення. Про хронічну токсичність, мутагенність і канцерогенність відомо мало.[1]
Джерела
- GESTIS Substance Database. gestis-database.dguv.de. Процитовано 24 листопада 2021.
- Booth, Gerald (15 червня 2000). У Wiley-VCH Verlag GmbH & Co. KGaA. Nitro Compounds, Aromatic. Ullmann's Encyclopedia of Industrial Chemistry (англ.). Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. с. a17_411. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a17_411.

